
Physique et Chimie : Tronc Commun
Semestre 2 Devoir 2 Modèle 1
Professeur : Mr EL GOUFIFA Jihad
Exercice 1 (4 pts)
On réalise deux circuits électriques dont les schémas sont les suivants :
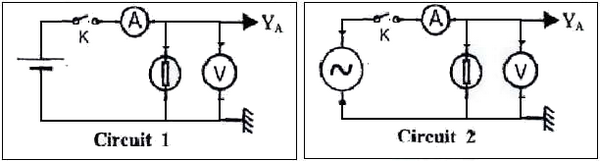
L’interrupteur K est fermé, on a effectué les réglages nécessaires pour obtenir à l’écran les oscillogrammes suivants :
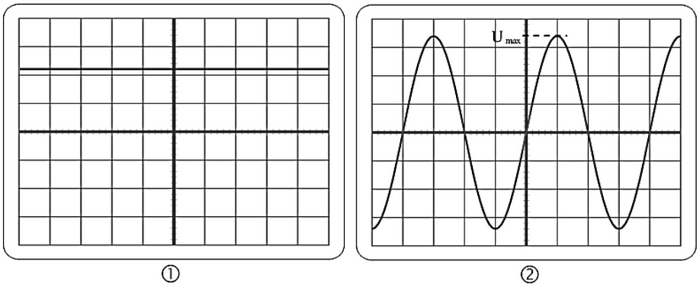
- Pour chaque oscillogramme, faire correspondre l’une des deux expressions suivantes : tension alternative sinusoïdale - tension continue.
On se place dans le cas du circuit 2 qui a permis d’obtenir l’oscillogramme 2.
La sensibilité verticale est de .
- Déterminer, à l’aide de l’oscillogramme 2, la valeur de la tension maximale .
- Le voltmètre indique une tension . Que représente ? calculer sa valeur.
La sensibilité horizontale est de .
- Déterminer, à l’aide de l’oscillogramme 2, la période du signal en puis en .
- En déduire la fréquence du signal.
Exercice 2 (4 pts)
Soit le circuit électrique suivant :
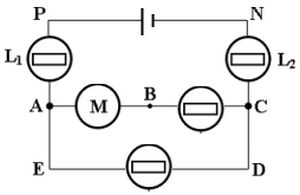
On donne : ; et
- Représenter, par une flèche sur le circuit les tensions , et .
On branche un voltmètre entre les bornes du générateur pour mesurer la tension .
- Représenter ce voltmètre sur le circuit en indiquant ses bornes.
Le calibre du voltmètre étant fixé à 30V et l’aiguille s’arrête devant la graduation sur l’échelle .
- Calculer la valeur de UPN. En déduire celle de UNP.
- Calculer .
Exercice 3 (5 pts)
On considère le circuit électrique suivant :
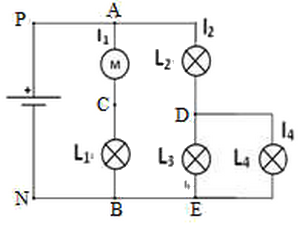
- Comment sont branchés la lampe et le moteur ?
- Combien de nœuds et de branches y a-t-il dans ce circuit ?
- Calculer la quantité d’électricité qui traverse le moteur pendant 15 minutes de fonctionnement, et en déduire le nombre d’électrons qui le traverse.
- Quelle est l’intensité de courant qui traverse la lampe ? Justifier.
- Calculer l’intensité du courant qui traverse la lampe .
- En déduire l’intensité qui traverse la lampe .
On donne :
- Les intensités du courant : ; et
- Charge élémentaire
Exercice 4 (7 pts)
Partie 1
Un comprimé contient de vitamine C (acide ascorbique ).
- Quelle est la masse molaire de l'acide ascorbique ?
- Quelle est la quantité de matière d'acide ascorbique dans un comprimé ?
- Combien y a-t-il de molécule d'acide ascorbique dans un comprimé ?
- Dans une molécule d'acide ascorbique, quels sont les pourcentages, en nombre d'atomes, des éléments chimiques , et ?
- Quel sont les pourcentages massiques des différents éléments chimiques constituant l'acide ascorbique?
L’orange contient d'acide ascorbique , on presse une orange moyenne et on recueille la masse en vitamine C.
- Combien d’oranges faudrait-il manger pour absorber autant de vitamine C que celle apportée par un comprimé ?
Partie 2
Une cartouche de gaz contient de butane à l’état liquide. Dans cet état, sa masse volumique est .
Lorsque l’on ouvre la cartouche, le butane change d’état physique et on le récupère à l’état gazeux.
- Calculer la masse de butane liquide dans la cartouche.
- Quelle est la quantité de matière de butane dans la cartouche ?
- Quel volume total de gaz peut-on espérer recueillir ?
Données
- Volume molaire des gaz


