
Physique et Chimie : 3ème Année Collège
Examen Local 3
Professeur : Mr El GOUFIFA Jihad
I- Exercice 1 (8 pts)
- Répondez par vrai ou faux et corrigez les phrases incorrectes :
- Le corps est ce qui fait la matière : ________
- L'atome se compose d'un noyau et d'un vide uniquement : ________
- Le plastique de type PS est soluble dans l'eau : ________
- Le métal qui ne réagit pas avec l'acide chlorhydrique ni avec la soude est le zinc : ________
- Encerclez la bonne réponse :
- Le cuivre se caractérise par :
Attiré par l'aimant / la couleur rouge brique.
- La formule chimique de l'oxyde de fer III est :
/
- L'oxydation de l'aluminium dans l'air donne une couche :
Imperméable / poreuse
- Lorsque vous versez la solution de soude sur un morceau d'aluminium, cela donne:
gaz dihydrogène / gaz dioxygène
- Reliez chaque ion à sa catégorie :
|
|
|
- Complétez la phrase suivante :
Le crayon est ___________________ se compose du plomb et de bois. Le plomb appartient au groupe de matériaux ________________________ car il est conducteur de la chaleur et d'électricité, contrairement au bois qui appartient au groupe des matériaux _________________ du fait qu'il contient de _________________ et d’hydrogène.
- Définissez la matière organique :
____________________________________________________________________________________________
____________________________________________________________________________________________
II- Exercice 2 (8 pts)
Partie 1
Le calcium Ca est un élément essentiel dans la construction des os et se trouve dans de nombreux aliments comme le lait et le poisson sous forme d'ions.
L'atome du calcium se transforme en ion en perdant deux électrons et son numéro atomique Z=20.
- Calculez la charge de l’atome.
- Calculez la charge du noyau.
- Écrivez le symbole de l'ion.
- Déterminez la charge des électrons de l’ion.
Partie 2
Un enseignant a préparé à six solutions aqueuses et a mesuré le pH de chacune d’elle et a noté les résultats suivants :
| La solution | Vinaigre | Acide chlorhydrique | Eau pur | Eau de chaux | Soude | Chlorure de sodium |
| Le pH | 5,3 | 1,8 | 7 | 10,4 | 12,8 | 7 |
|
La nature |
- Nommez l’instrument utilisé pour mesurer le pH de ces solutions en justifiant votre réponse.
- Remplissez le tableau ci-dessus, en identifiant la nature de chaque solution.
- Déterminez :
- La solution la plus acide : ____________________
- La solution la plus basique: ____________________
Le professeur a ajouté une solution de soude à l'eau pure.
- Nommez cette technique.
- Le pH de la solution va-t-il augmenter ou diminuer après cette technique ?
Le professeur a versé un peu d'acide chlorhydrique dans un tube à essai contenant du fer et a rapproché la flamme à son orifice, comme le montre le schéma suivant :
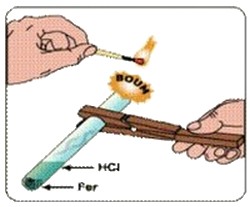
- Nommez le gaz produit et écrivez sa formule.
- Donnez le nom et la formule de l’ion produit. Comment on le détecte ?
- Écrivez l'équation simplifiée de la réaction réalisée par le professeur.
III- Exercice 3 (4 pts)
Les micronutriments sont des médicaments qui contiennent des ions, et sont prescrits pour compenser le manque (la carence) dans le corps du patient.
Le docteur a prescrit à Salma ces nutriments sous forme de comprimé, elle a oublié d’attirer son attention qu'elle est Allergique au fer et au chlore.
Elle voulait savoir si elle pouvait prendre ces médicaments sans effets secondaires.
Salma a pris un comprimé et l'a dissout dans l'eau, puis elle a pris deux échantillons :
- Elle a Ajouté au première échantillon, des gouttes de la solution hydroxyde de sodium, qui a produit un précipité vert.
- Elle a ajouté au deuxième échantillon, des gouttes de la solution nitrate d’argent, qui a produit un précipité blanc noircit sous l'influence de la lumière.
- Quels sont les ions détectés ?
- Écrivez l’équation de précipitation dans chaque échantillon.
- Salma peut-elle prendre ces comprimés sans effets secondaires ? Justifiez votre réponse.


